ARTROSCOPIA | VOL. 23, Nº 3 : 93-105 | 2016
ACTUALIZACIÓN
Reconstrucción Artroscópica con Doble Banda del Ligamento Cruzado Posterior
Jorge Chahla1, Damián Arroquy2, Javier Olivetto2, Kaitie Whitney1, Robert F. LaPrade1,3
1- Steadman Philippon Research Institute. 2- Hospital Británico de Buenos Aires. 3- The Steadman Clinic.
Jorge Chahla
Esta dirección de correo electrónico está siendo protegida contra los robots de spam. Necesita tener JavaScript habilitado para poder verlo.
RESUMEN
En la actualidad, la comprensión de las opciones diagnósticas y de tratamiento para el ligamento cruzado posterior (LCP) han evolucionado, dando lugar a resultados clínicos superiores. Asimismo, distintos autores han publicado resultados que varían desde buenos a excelentes tras el tratamiento no quirúrgico de lesiones aisladas del LCP. Sin embargo, datos recientes hacen referencia a la disminución de las puntuaciones clínicas y la aparición de artrosis precoz en lesiones aisladas severas o combinadas del LCP tratadas de forma conservadora. Por lo anteriormente mencionado se ha vuelto a considerar el tratamiento quirúrgico para muchas de estas lesiones. Durante la última década, se han realizado varios estudios para evaluar la eficacia de las reconstrucciones de simple versus doble banda. Sin embargo, la literatura no es concluyente con respecto a la superioridad de una técnica sobre la otra. El objetivo de este estudio fue revisar los principios básicos de la anatomía del LCP, su biomecánica, su diagnóstico y tratamiento, haciendo hincapié en la reconstrucción del LCP con doble banda femoral y tibial.
Palabras claves: Ligamento Cruzado Posterior; Anatomía; Reconstrucción; Doble Banda
ABSTRACT
Currently, diagnostic understanding and treatment options for the posterior cruciate ligament (PCL) have evolved, resulting in superior clinical outcomes. Also different authors have reported results ranging from good to excellent after nonsurgical treatment of isolated PCL injuries, but new studies refer to decreased clinical scores and early osteoarthritis in severe or combined isolated PCL injuries treated conservatively, prompting surgeons to consider operative intervention in many cases. Over the past decade, there have been several studies to assess the effectiveness of single versus double band reconstructions. However, the literature is inconclusive regarding the superiority of one technique over the other. The aim of this study was to review the basic principles of PCL anatomy, biomechanics, diagnosis and treatment, emphasizing PCL reconstruction with double femoral and tibial band.
Keywords: Posterior Cruciate Ligament Anatomy; Reconstruction; Double-band
INTRODUCCIÓN
En las últimas dos décadas, la comprensión de las opciones diagnósticas y de tratamiento para el ligamento cruzado posterior (LCP) han evolucionado, dando lugar a resultados clínicos superiores.
Históricamente, distintos autores han publicado resultados que varían desde buenos a excelentes tras el tratamiento no quirúrgico de lesiones aisladas del LCP.1,2 Sin embargo, nuevos estudios hacen referencia a la disminución de las puntuaciones clínicas y la aparición de artrosis precoz en lesiones aisladas severas o combinadas del LCP tratadas de forma conservadora,3-5 por lo que se ha vuelto a considerar el tratamiento quirúrgico para muchas de estas lesiones.
El objetivo de este estudio fue revisar los principios básicos de la anatomía del LCP, su biomecánica, su diagnóstico y tratamiento, haciendo hincapié en la reconstrucción del LCP con doble banda femoral y tibial.
ANATOMÍA
El LCP se origina en la cara lateral del cóndilo femoral medial, precisamente en la unión de la pared medial y el techo de la escotadura intercondílea. Luego se dirige hacia posterior y lateral para insertarse en una depresión en la cara posterior de la tibia, rodeada por una prominencia medial y otra lateral (fig. 1).1,6
El ligamento mide de 32 a 38 mm de longitud, con un ancho promedio de 13 mm.1,6 La zona media del ligamento es la más compacta, y comprende aproximadamente un tercio del diámetro de las inserciones femoral y tibial con una media de 11 mm de ancho.7 Aunque el LCP se encuentra dentro de la cápsula articular de la rodilla, se lo considera extra-articular, ya que está encerrado dentro de su propia vaina sinovial.8
Funcionalmente, el LCP se puede dividir en tres porciones basadas en los patrones de tensión. Hay dos partes principales, o haces: uno anterolateral más grande (AL) y otro más pequeño posteromedial (PM).6,9,10 Además encontramos un tercer haz que corresponde a los ligamentos meniscofemorales: el anterior (ligamento de Humphry) y el posterior (ligamento de Wrisberg) (fig. 2).7,11
El haz AL actúa como estabilizador primario a la traslación posterior y está bajo mayor tensión cuando la rodilla está en 90° de flexión.12-15 Es aproximadamente dos veces más grande en área de sección transversal que el haz PM.7,16 En contraste, el haz PM proporciona estabilidad en la traslación posterior cuando la rodilla se acerca a la extensión completa (por lo que es el estabilizador primario en extensión de la rodilla) y se ha observado que también funciona como estabilizador secundario en la rotación.17,18 Por lo tanto, la tensión se desarrolla de una manera recíproca en cada haz durante el rango de movimiento de la rodilla, con pocas fibras que muestran un comportamiento isométrico.
Figura 1: Vista posterior de una rodilla derecha cadavérica mostrando los reparos óseos y de tejido blando del ligamento cruzado posterior (LCP). AL: haz anterolateral, PM: haz posteromedial.
Figura 2: Vista lateral de una rodilla derecha (hemiseccionada) que demuestra la inserción femoral del haz anterolateral (AL), el haz posteromedial (PM), y el ligamento meniscofemoral posterior de Wrisberg.
BIOMECÁNICA DEL LIGAMENTO CRUZADO POSTERIOR
El LCP proporciona el sistema de retención primario de la traslación posterior de la tibia.12 La fuerza al fallo para el haz AL es de 1.120 ± 362 N, que es casi tres veces más que la del haz PM (419 ± 128 N).7
Markolf y cols. observaron que la cinemática de la rodilla se mantiene casi normal cuando el haz de AL se conservó y el haz PM se seccionó, por lo tanto, sugirieron que el haz AL debe ser el foco de la reconstrucción tradicional con una sola banda.14,19 Sin embargo, Kennedy y cols. encontraron resultados similares cuando el haz de AL se seccionó y el haz PM fue dejado intacto, lo que sugiere que ambos haces tienen una acción codominante.20
Es importante destacar que los estudios biomecánicos han comprobado que el LCP es una estructura no isométrica con tensión desigual en todo el movimiento de la rodilla.21 Las fuerzas de cizallamiento aumentan a 300 de flexión y son mayores en ángulos de flexión superiores a 50°-60°.22-24 La longitud del LCP también aumenta cuando la rodilla está bajo carga en flexión de 0–90°,23,25-27 luego permanece relativamente constante de 105°–120°, y después disminuye de 120°-135°.25,27
Por último, se ha demostrado que el LCP desempeña un papel en la estabilidad rotacional y sobre todo en los ángulos de flexión más altos.20,29 Estudios biomecánicos han demostrado una restricción significativa del LCP a la rotación interna a partir de los 90° de flexión.20,29 Más específicamente, el haz PM desempeña un papel pertinente en el mantenimiento de la estabilidad posterior en un rango completo de movimiento y en la estabilidad rotacional más allá de los 90° de flexión, lo que sugiere que las reconstrucciones de simple banda que no reconstituyen el haz PM no pueden restaurar la estabilidad posterior completa y la rotacional en comparación con una técnica de doble banda.20,29
DIAGNÓSTICO
Cuando se evalúa un paciente con sospecha lesión de ligamento cruzado posterior, es importante evaluar la totalidad de la rodilla en términos de estabilidad, el estado nervioso y vascular para evitar pasar por alto lesiones asociadas. Esto es especialmente importante si hay una historia de luxación de la rodilla, que tiene un mayor riesgo de lesión neurovascular.
En cuanto al LCP, hay 4 pruebas específicas que se deben realizar para determinar la integridad del ligamento: el cajón posterior, el hundimiento posterior, la prueba activa del cuádriceps y la prueba de rotación interna en decúbito supino (RI).
La prueba del cajón posterior se lleva a cabo con la rodilla en 90° de flexión y es la más útil para la documentación de la insuficiencia del LCP. En este ángulo de flexión, los cóndilos tibiales anteriores se deben colocar anterior a los cóndilos femorales (aproximadamente 10 mm) en una rodilla normal. Si la tibia se puede mover posteriormente 0-5 mm en el lado lesionado, esto se considera un grado I y por lo general corresponde al desplazamiento posterior de los cóndilos tibiales a una posición que todavía es anterior a los cóndilos femorales. Si la tibia se puede desplazar de 5 a 10 mm posteriormente, esto es un signo del cajón posterior grado II, que corresponde al desplazamiento posterior de los cóndilos tibiales hasta el mismo nivel que los cóndilos femorales. Si la tibia se puede desplazar más de 10 mm posteriormente, o posterior a los cóndilos femorales, esto representa un grado III.
La prueba de hundimiento posterior se lleva a cabo con la cadera y la rodilla a 90° de flexión, utilizando la gravedad para aplicar fuerza dirigida posteriormente a la tibia. El hundimiento posterior de la tibia en el lado lesionado se compara con el lado no lesionado. La diferencia en el desplazamiento posterior de la tibia sugiere la lesión del LCP.
La prueba activa del cuádriceps también es útil en el diagnóstico de las lesiones de LCP. Esta prueba consiste en colocar al paciente en decúbito supino y flexionando las rodillas a 90º con el pie apoyado sobre la mesa. En la rodilla intacta, una contracción del cuádriceps resulta en la traslación posterior de la tibia con respecto al fémur. En la rodilla con LCP deficiente, la tibia se encuentra en una posición de subluxación posterior, y una contracción del cuádriceps produce la traslación anterior de la tibia con respecto al fémur. Por lo tanto, la traslación anterior con la contracción del cuádriceps con la rodilla en flexión de 90° sugiere la lesión del ligamento cruzado posterior. Se cree que la prueba activa del cuádriceps y la prueba del cajón posterior son las más útiles para el diagnóstico de lesión del ligamento cruzado posterior.
Por último, la prueba de RI en posición supina fue recientemente descripta como un posible adyuvante para el diagnóstico de las lesiones del LCP.30 La prueba se realiza mediante la evaluación de la rotación interna de la tibia en comparación con la pierna contralateral en distintos ángulos de flexión. Un estudio reciente reportó una sensibilidad del 95,5%, una especificidad del 97,1%, un valor predictivo positivo del 72,4% y un valor predictivo negativo del 99,6% para el diagnóstico de las lesiones grado III del LCP.30 La lesión del complejo posteroexterno presenta una interacción significativa con el prueba de RI en decúbito supino, aumentando su sensibilidad y la disminuyendo su especificidad.
Radiografías con Estrés
Cuando estamos en presencia de una potencial inestabilidad posterior, las radiografías con estrés son un complemento útil y reproducible para ayudar a cuantificar la inestabilidad.31 Según lo descrito por Jackman y cols.,31 la radiografía con estrés permite la comparación del grado de desplazamiento posterior entre las rodillas lesionadas y no lesionadas. Desde un punto de vista técnico, un soporte a 90° ha sido construido para asegurar el posicionamiento cómodo, estable y reproducible del paciente durante la radiografía. Este consiste en un brazo horizontal ligeramente acolchado y una extremidad vertical perpendicular al suelo. El brazo horizontal soporta la pierna desde la tuberosidad anterior de la tibia hacia distal, con la rótula y cóndilos femorales libres sobre el borde. El brazo vertical se asegura de que la rodilla está flexionada a 90°. Los pacientes son instruidos para apoyar su peso sobre sus tuberosidades tibiales y no colocar ningún peso sobre la rótula para proporcionar una fuerza posterior. Se les permite estabilizarse por si mismos en una estructura de soporte frente a ellos (fig. 3).
Figura 3: Paciente en el soporte de apoyo para realizar las radiografías con estrés para una rodilla izquierda. Se instruye al paciente para poner todo el peso sobre la tuberosidad anterior de la tibia, mientras se obtiene la radiografía. Las manos pueden estar apoyadas en una baranda. Reproducido con permiso de Jackman T, La Prade RF, Pontinen T, Lender PA: la fiabilidad intraobservador e interobservador de la técnica de la radiografía de rodillas con estrés para la evaluación de la laxitud posterior de la rodilla. Am J Sports Med 2008, 36 (8): 1571-1576.
En la radiografía lateral, a continuación se identifica un punto a lo largo de la cortical posterior de la tibia a 15 cm distal a la línea articular. Se dibuja una línea a partir de ese punto paralelo a la cortical posterior, que pase a través de los cóndilos femorales, y se marca el punto más posterior de la línea de Blumensaat’s (fig. 4).
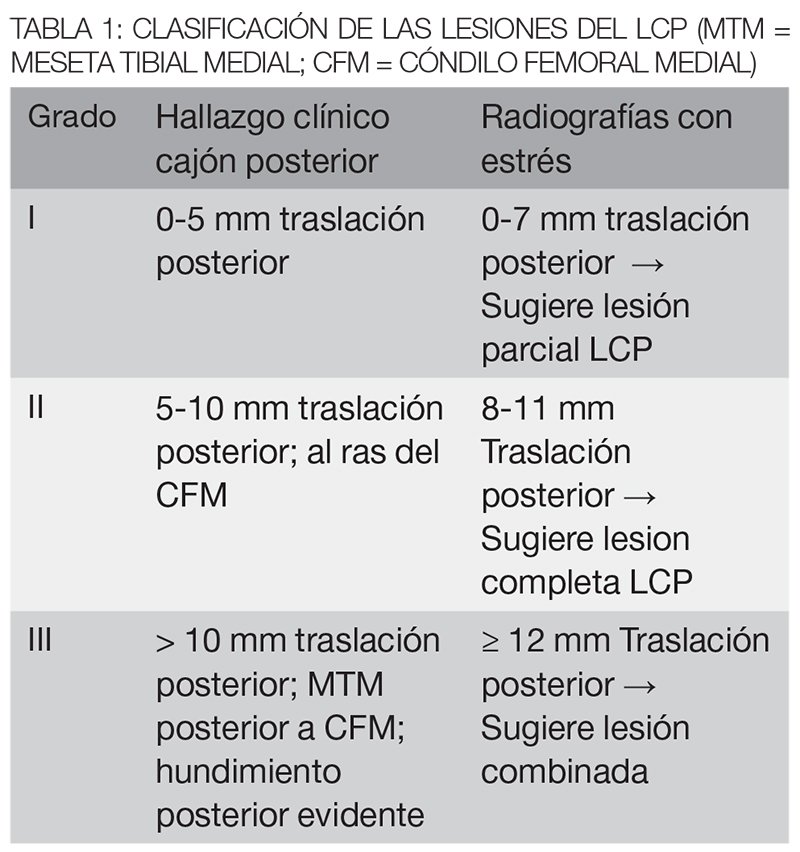
Una línea perpendicular se dibuja desde ese punto hasta intersectar la primera línea, y esta distancia se compara con el lado contralateral (fig. 5).31 La Tabla 1 muestra los valores que ayudan a diferenciar los diferentes grados de lesiones del LCP.
Figura 4: Radiografía lateral de rodilla con estrés en una rodilla derecha que demuestra el método de medición. En primer lugar, un punto se identifica a lo largo de la cortical posterior de la tibia a 15 cm de la línea de la articular y se dibuja una línea desde ese punto paralelo a la cortical posterior, pasando a través de los cóndilos femorales (línea discontinua). Se marca el punto más posterior de la línea de Blumensaat’s y luego se dibuja y se mide una línea perpendicular que conecta este punto a la línea hecha previamente.
Figura 5: Radiografías de perfil con estrés de rodillas comparativas que demuestren una diferencia de 10 mm sugestiva de una lesión del LCP.
TRATAMIENTO
Indicaciones
El enfoque para el tratamiento de las lesiones del LCP debe tener en cuenta varios factores específicos del paciente, incluyendo: la gravedad de la lesión (aislada vs combinado), el grado de lesión del ligamento cruzado (tabla 1), el tiempo (aguda o crónica), la presentación clínica (asintomática vs dolor/inestabilidad), y la demanda funcional del paciente o el nivel de actividad (deportista vs sedentaria).32 Debido a la controversia en torno a la historia natural de la deficiencia de LCP y las dificultades para reconstruir con precisión la compleja función del LCP quirúrgicamente, no hay un consenso claro respecto a las indicaciones para la reconstrucción del LCP. La mayoría de los autores están de acuerdo en que las fracturas por avulsión del LCP deben ser reparadas de forma aguda con puntos de sutura o tornillo de fijación, generalmente con buenos resultados.33-35 Además, las lesiones múltiples del LCP con LCA, CPE, o LCM deben ser quirúrgicamente reconstruidas, preferentemente dentro de las 2-4 semanas de la lesión para restaurar la función de la rodilla.32,36,37 Sin embargo, el algoritmo de tratamiento debe adaptarse a cada paciente.
En general, las lesiones agudas y aisladas del LCP (grados I y II) se tratan de forma conservadora. Para clasificar una lesión del ligamento cruzado como “aislado”, se han reportado tres criterios para considerar tratamiento incruento.38 Estos incluyen: 1) radiografías de estrés con LCP con una diferencia <12 mm en comparación con la rodilla contralateral; 2) <5 grados de laxitud rotatoria anormal a los 30 grados de flexión de la rodilla; y 3) ninguna lesión de los ligamentos colaterales significativa que cause inestabilidad en varo o valgo. Si una lesión del ligamento cruzado cumple estos tres criterios, se puede considerar “aislado”, y si se les da una calificación de I o II en la exploración física, el paciente debe someterse a un tratamiento no quirúrgico. La mayoría de estos pacientes son capaces de volver a practicar deportes dentro de las 4-6 semanas después de la lesión.
Por el contrario, el tratamiento de las lesiones aisladas del LCP grado III y agudas es controversial. En general, los autores intentan tratar estas lesiones de forma no quirúrgica con un periodo de inmovilización seguido de rehabilitación. Debido al riesgo de una lesión oculta del complejo posteroexterno (CPE) de la rodilla, se recomienda que la rodilla se inmovilice en extensión durante 2-4 semanas seguido de una férula dinámica durante 3 meses. La curación elongada del LCP puede conducir a la inestabilidad y discapacidad crónica.9 El uso de una férula que aplique una fuerza de cajón anterior, ha demostrado que al colocar el LCP en una posición adecuada con menor cajón posterior permite mejorar su curación.40 Además, la inmovilización en extensión disminuye la tensión sobre las fibras anterolaterales del LCP y el CPE, facilitando la curación al minimizar la traslación tibial posterior secundaria a la disminución de la tensión por parte de la gravedad y de los isquitibiales.37 Después del período inicial de inmovilización, comienza la rehabilitación, pero no todos los pacientes con lesiones grado III se recuperan y un gran porcentaje requiere finalmente la reconstrucción de LCP.38,40,41 Del mismo modo, las lesiones del LCP combinadas y agudas (es decir, LCP / CPE) frecuentemente conducen a limitaciones funcionales y artrosis precoz.42,43 Por lo tanto, la reconstrucción quirúrgica se recomienda en estos casos.
En el contexto de una rotura crónica del LCP, los autores eligen como tratamiento para los grado I y II una conducta conservadora, similar a una lesión aguda. Los pacientes sintomáticos con inflamación recurrente y dolor se tratan con modificación de la actividad y fisioterapia, ya que en este punto, la reconstrucción quirúrgica de lesiones crónicas o agudas grado I y II no ha obtenido mejorías significativas en los síntomas o función.37 En contraste a lo expresado anteriormente, el tratamiento no quirúrgico de lesiones crónicas grado III o lesiones del LCP combinadas produciría secuelas a largo plazo con limitación funcional y el posible desarrollo artrosis temprana.3,4 Los pacientes a menudo se quejan de dolor persistente, de inestabilidad y la pérdida de función en el seguimiento a largo plazo con el tratamiento no quirúrgico de estas lesiones. También se han descripto peores resultados en pacientes que han aumentado el tiempo entre la lesión inicial y el tratamiento quirúrgico.35,40 Por lo tanto, en los casos de lesiones crónicas del LCP grado III o lesiones combinadas con síntomas persistentes de dolor o inestabilidad a pesar del tratamiento conservador, se recomienda el tratamiento quirúrgico.
Tratamiento quirúrgico
El objetivo principal de la reconstrucción del LCP es restaurar la anatomía y la función normal. En la actualidad, no existe un “patrón de oro” para la reparación o reconstrucción que proporcione consistentemente resultados buenos o excelentes. En los casos de avulsión ósea aguda del LCP, la intervención quirúrgica está indicada.44 Las fracturas por avulsión por lo general implican la inserción tibial y constituyen la única indicación para una reparación primaria LCP. La reparación se debe hacer en el período agudo (menos de 3 semanas), y puede ser realizado con tornillos y arandelas, sutura, o técnicas de banda de tensión.33-35 En contraste con las avulsión óseas, los resultados de la reparación de lesiones a nivel del ligamento ya sean agudos o crónicos han sido pobres, por lo que en estos casos se recomienda la reconstrucción.45
Se han descrito varios métodos diferentes de reconstrucción del LCP. Debido a la complejidad de los patrones de tensión de los dos haces, ha sido difícil reproducir la función y la posición nativa del complejo ligamentario. Las técnicas actuales incluyen la incrustación tibial, artroscópica transtibial con una sola banda y artroscópica transtibial con doble banda. En este capítulo se hará hincapié en la técnica con doble banda.
Quizás el tema más controvertido en la reconstrucción artroscópica del LCP es si se debe reconstruir una o dos de las bandas. En comparación con el haz PM, el haz AL es más rígido y por lo tanto tiene una carga de rotura superior. Además es aproximadamente el doble del ancho del haz PM y sirve como base para la reconstrucción con una sola banda.18
RECONSTRUCCIÓN ARTROSCÓPICA CON DOBLE BANDA
Consideraciones anatómicas
La reconstrucción de doble banda es un intento de reproducir los dos haces del LCP y lograr una reconstrucción más “anatómica”, en oposición a la reconstrucción con una sola banda donde solo se reconstruye el haz AL.46
En el fémur, el LCP tiene una huella amplia (32 mm diámetro), relativamente vertical en la cara anterolateral del cóndilo femoral medial, a 7-8 mm proximal a la superficie articular desde su punto medio (fig. 6).47,48
En un estudio cadavérico reciente, en el 75% de las muestras (n=20) se observó una forma semicircular de la huella femoral, mientras que el 25% tenían una forma oval.10 Los autores observaron que la superficie de la huella femoral era de 209 ± 33.82 mm2, siendo 118 ± 23.95 mm2 para el haz AL y 90 ± 16.13 mm2 para el PM49,50 la distancia media entre los centros del haz AL y PM es de aproximadamente 12,1 mm (+/- 1,3). Los márgenes distales de los haces AL y PM son de 1,5 mm (+/- 0,8) y 5,8 mm (+/- 1,7) proximal al cartílago articular respectivamente.51
Históricamente, se utilizó un método horario para identificar la colocación del túnel durante la intervención.32,52 Evidencia reciente, sin embargo, sugiere que el método de reloj tiene poca precisión clínica y reproducibilidad.53 Anderson y cols. disecaron 20 rodillas de cadáveres humanos frescos congelados para determinar mejor las referencias artroscópicas para la colocación de los túneles en la técnica de doble banda.51 En el fémur el centro del túnel del haz AL debe ser triangulado sobre la base del punto troclear, el punto del arco medial y la prominencia bifurcada medial, mientras que el borde distal debe ser colocado adyacente al cartílago articular. Por otro lado el centro del túnel femoral del haz PM debe ser colocado equidistante desde el punto posterior y el punto del arco medial, inmediatamente distal a la cresta intercondilar medial, con un promedio desde el centro de 8,6 mm proximal al margen del cartílago articular. Debe respetarse una distancia media entre el haz AL y PM de 12,1 mm, por lo que la utilización de un túnel AL de 11 mm diámetro y un túnel PM de 7 mm todavía permitiría un puente óseo de 3 mm entre los dos túneles femorales. Como se ilustra en la figura 7, el haz anterolateral (inserción más grande) es más proximal que la huella posteromedial (inserción más pequeña) en el cóndilo femoral medial. En un análisis cuantitativo de los sitios de inserción, Harner y Baek identificaron el área de inserción femoral del LCP de aproximadamente 128 mm2, que es lo suficientemente grande como para dar lugar a ambos túneles.49
En contraste con la inserción femoral, la inserción tibial del LCP es más compacta.8,50,54 Los dos haces se insertan en la tibia sin separación anatómica en una fóvea, situada en la cara posterior de la tibia en una depresión entre la meseta tibial lateral y medial.6,55 Recientemente, Anderson y cols. Informaron que la distancia media entre los centros de los haces AL y PM fue de 8,9 mm (+/- 1,2).51 Las fibras blancas nacaradas del cuerno posterior del menisco medial sirven como el borde anterior de la huella tibial del LCP, mientras que la cresta define consistentemente el margen posterior del haz AL y el margen anterior del haz PM.51 El centro de los dos haces se encuentra aproximadamente en el 48% del ancho mediolateral de la meseta tibial desde medial.55
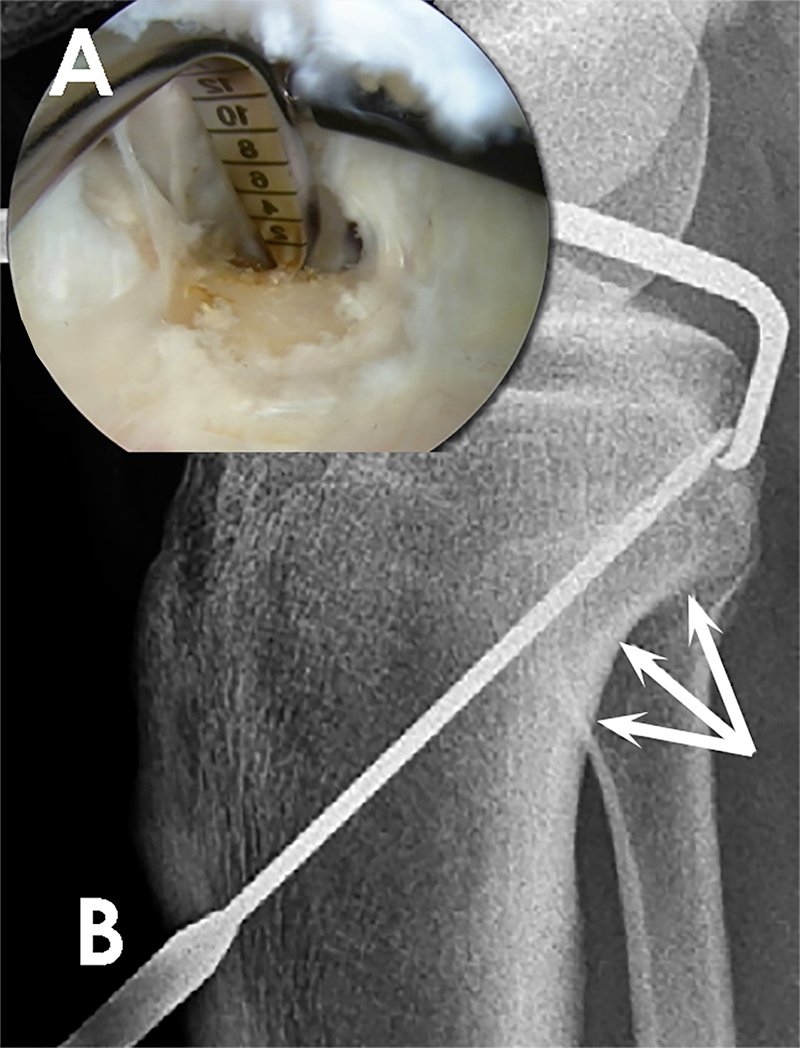
Basado en el trabajo de Anderson,51 el centro del túnel tibial debe colocarse anterosuperior a la cresta, en el lado medial de la faceta del LCP, a 9,8 mm del punto de cartílago lateral, y 5,0 mm de la fóvea medial.51 Una imagen artroscópica intraoperatoria y una radiografía lateral (fig. 8, A y B) demuestran la posición apropiada de la guía del túnel tibial.
Esto corresponde a un cuarto del total de la faceta a la corteza tibial posterior (es decir, 7 mm anterior a la corteza posterior).56 La colocación del túnel más posterior o inferiormente fallará para reproducir la anatomía normal y corre riesgo de lesión neurovascular del paquete poplíteo, que se encuentra en las proximidades de ligamento. A su vez, la colocación del túnel más anterior puede comprometer las raíces meniscales posteriores.
Figura 6: Imagen cadavérica que muestra la inserción femoral del LCP y la relación con el cartílago de los 2 haces en una rodilla derecha (AL: haz anterolateral y PM: haz posteromedial).
Figura 7: Imagen artroscópica (portal anterolateral) de una rodilla izquierda que representa el posicionamiento de los túneles femorales. Debe existir un puente de hueso de al menos 2 mm entre los dos túneles. ALB: haz anterolateral, PMB: haz posteromedial.
Figura 8: Imagen artroscópica. A) demuestra la posición deseada de la guía de LCP en la inserción tibial. B) radiografía lateral intraoperatoria que muestra la ubicación de la guía a 6-7 mm proximal a la imagen en “copa de champán” en la faceta del LCP.
Técnica quirúrgica
La técnica artroscópica de doble banda transtibial que se describe aquí fue descripta inicialmente por Spiridonov, LaPrade y cols.58 La técnica utiliza dos injertos fijos en túneles femorales divergentes, que pasan por un único túnel tibial y se fijan por separado en la tibia para recrear los dos haces anatómicos del LCP.
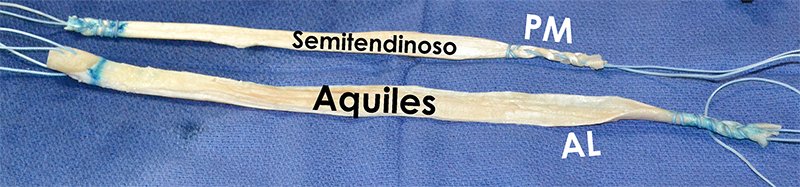
En primer lugar, los portales artroscópicos estándar pararotuliano inferomedial e inferolateral se hacen adyacente al tendón rotuliano. El injerto para reconstruir el haz AL se prepara a partir de un aloinjerto de tendón de Aquiles con 11 mm de diámetro, un taco óseo de hueso del calcáneo de 25 mm de longitud y el aspecto de los tejidos blandos distales del injerto es tubularizado con una sutura reabsorbible número-2. El injerto para el haz PM se prepara de forma similar a partir de un aloinjerto de tejido blando de 7 mm de diámetro (semitendinoso o aloinjerto de Aquiles) (fig. 9).
Los túneles femorales se realizan en primer lugar. Se identifican los orígenes anatómicos de los haces AL y PM y se marca el centro de cada túnel provisoriamente con un coagulador artroscópico (fig. 10).51
Para el túnel femoral AL, se coloca a través del portal artroscópico antero lateral una fresa de 11 mm de diámetro y se utiliza como una guía del túnel. Se coloca en el centro previamente marcado, teniendo en cuenta los márgenes del cartílago articular, la parte superior del techo del intercóndilo y la cara anterior del cóndilo femoral medial. Se realiza la perforación anteromedial con una clavija guía con ojal a través de la fresa (fig. 11).
Figura 9: Fotografía quirúrgica mostrando la preparación de los aloinjertos para la reconstrucción de las dos bandas de lLCP. AL: anterolateral, PM: posteromedial.
Figura 10: Un coagulador artroscópico se utiliza para delimitar ambos túneles femorales en las ubicaciones deseadas. Se observa la imagen artroscópica (izquierda) a través del portal anterolateral de una rodilla derecha.
Figura 11: En una rodilla derecha, una fresa de 11 mm se coloca en el centro del haz AL con el borde contra los márgenes del cartílago articular en la parte superior del techo intercondilar, y a lo largo de la cara anterior del cóndilo femoral medial ( izquierda). Con una clavija con ojal se perfora luego a través de la fresa usándola como guía (derecha).
Luego se realiza un túnel cerrado de 11 x 25 mm sobre la clavija guía. Un hilo de sutura se pasa través de una clavija con ojal.
Para el túnel femoral PM, se utiliza una técnica similar. Se utiliza una fresa de 7 mm colocándola contra el contorno del haz posteromedial, con el borde distal de la fresa a 5 mm proximal aproximadamente al borde distal del cartílago articular del cóndilo femoral medial y ligeramente posterior al túnel del haz AL (fig. 7). Luego se perfora con una clavija con ojal a través de la fresa. Se realiza un orificio de 25 mm de longitud de forma divergente y se pasa una sutura dentro del ojal. Es importante conservar un puente óseo de 2-3 mm entre los dos túneles.
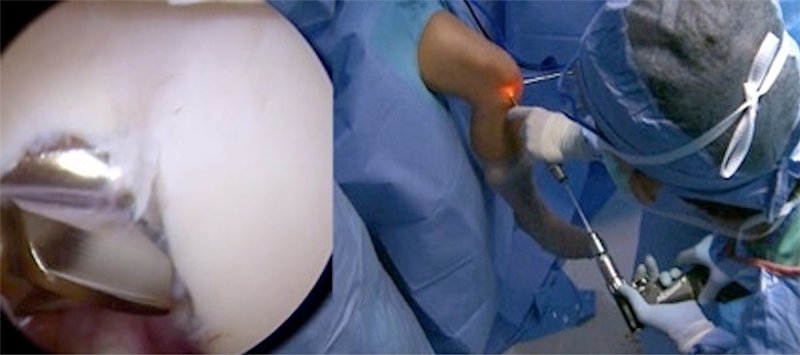
A la hora de realizar el túnel tibial, se coloca una óptica de 70 grados para facilitar la visualización. En primer lugar, se coloca un shaver a través del portal artroscópico posteromedial para desbridar la inserción tibial del LCP. El desbridamiento distalmente a lo largo de la faceta LCP se debe realizar hasta que se visualicen las fibras del músculo poplíteo. Es importante en este punto tener cuidado para evitar el desbridamiento demasiado agresivo, ya que las estructuras neurovasculares están posterior a la cápsula. A continuación, una clavija guía se perfora a través de la tibia usando una guía de LCP, entrando en la cara anteromedial de la tibia aproximadamente 6 cm distal a la línea de la articulación, centrada entre la tuberosidad anterior y el borde medial de la tibia. El objetivo es salir posteriormente en la inserción tibial del LCP justo distal y lateral a las fibras blancas del menisco medial (fig. 12).
En este momento se utiliza radioscopia (perfil) para verificar la ubicación correcta de la clavija guía, como describió Johanssen y cols.,57 aproximadamente 6 a 7 mm proximal a la imagen en copa de champagne en la faceta del LCP en la parte posterior de la tibia (fig. 8). A continuación, una fresa de 12 mm se utiliza para fresar bajo visualización artroscópica directa. Durante este paso, se inserta a través del portal posteromedial una cureta para alejar los tejidos posteriores de la fresa y proteger la progresión de la punta de la guía. A continuación, una raspa flexible se pasa hacia proximal por el túnel tibial y se la toma con una pinza desde el portal anteromedial. Con esta última se regulariza la apertura del túnel tibial intra-articular, para eliminar los restos óseos, que podrían interferir con el paso del injerto. Luego el extremo de este dispositivo se retoma por el portal anterolateral.
El injerto del haz PM se pasa primero por su respectivo túnel femoral a través del portal artroscópico anterolateral y se fija con un tornillo interferencial bioadegradable de 7 mm de diámetro. A continuación se coloca el taco óseo del injerto del haz AL, pasándolo de manera similar en su túnel femoral y se fija con un tornillo interferencial de titanio de 7 mm. Luego las suturas de los extremos de ambos injertos se pasan a través del bucle de la raspa (fig. 13).
La raspa con las suturas de los injertos en su ojal se tira distalmente por el túnel tibial y los injertos se pasan por el túnel tibial. Una vez los injertos en la cara anteromedial de la tibia se individualizan y se tensa el haz AL fijándolo primero con un tornillo de 4,5 mm con una arandela de 16 mm con púas manteniendo la rodilla flexionada a 90°, en rotación neutra, con una fuerza de reducción anterior a la tibia y la tracción distal aplicada al injerto (fig. 14).59
El haz PM se fija a la tibia con la rodilla en extensión completa con un tornillo de 4,5 mm con una arandela de 14 mm con púas colocada 2 cm aproximadamente a distal del primer tornillo, mientras se realiza tracción desde el injerto. La fijación del injerto PM a 0° y del injerto AL a 90° han demostrado una disminución significativa de la laxitud de la rodilla y de la carga del injerto en comparación con el estado seccionado y otros ángulos de fijación.59 La verificación artroscópica confirma que el ligamento cruzado anterior (LCA) se ha reducido a su posición normal y el LCP se observa en toda la amplitud de movimiento. Además, se chequea la restauración del cajón posterior a los 90° de flexión de la rodilla.
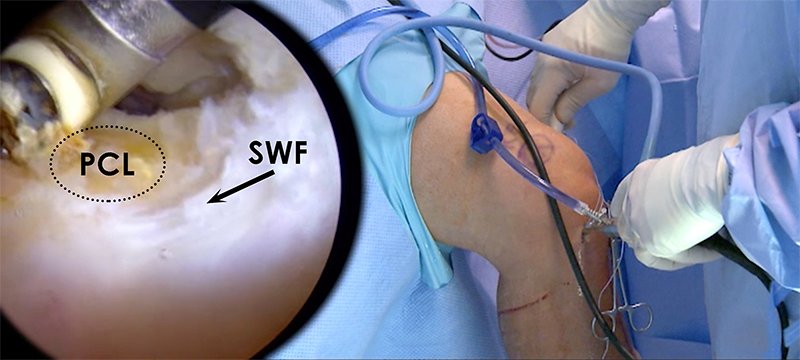
Figura 12: Imagen artroscópica (izquierda) que demuestra el lugar de la inserción tibial PCL y su relación con las fibras blancas y brillosas(SWF)de la raíz meniscal en una rodilla derecha. Un portal posteromedial debe ser creado para facilitar la preparación del túnel tibial (derecha).
Figura 13: Imagen quirúrgica mostrando los puntos de sutura de los extremos de ambos injertos pasados a través de la punta del bucle de la raspa flexible.
Figura 14: El haz AL se fija a la tibia con un tornillo de 4,5 mm con una arandela de 16 mm con púas manteniendo la rodilla flexionada a 90 grados, en rotación neutra, con una fuerza de reducción anterior de la tibia y tracción distal aplicada al injerto (derecha rodilla).
REHABILITACIÓN POSTOPERATORIA
Después de la operación, todos los pacientes se mantienen sin carga de peso durante seis semanas. La fisioterapia hace hincapié en la activación del cuádriceps y la flexión de la rodilla de 0° a 90°. Además, se coloca una férula ortopédica que idealmente debe ejercer una fuerza anterior a la tibia (por ejemplo: Jack Brace, Ossur Rebound Brace) la cual se debe usar en todo momento. Debe evitarse cualquier ejercicio que active los isquiotibiales en las fases iniciales de la rehabilitación.60,61 Seis semanas después de la operación, los pacientes inician la carga de peso. Se inicia el uso de una bicicleta fija con baja resistencia y prensa de la pierna a un máximo de 70° de flexión de la rodilla. Los aumentos adicionales de los ejercicios de bajo impacto son permitidos según la tolerancia, a partir de las doce semanas.
Seis meses después, los pacientes son evaluados clínicamente y con radiografías con estrés de forma rutinaria. Si existe evidencia objetiva de la adecuada curación o ligamentización de la reconstrucción (<2 mm de aumento de la traslación posterior en comparación con la rodilla contralateral), los pacientes deben suspender el uso de la férula, con la excepción de los pacientes con >2 mm de aumento de la traslación posterior, una revisión de LCP, o presentar un índice de masa corporal (IMC) >35 kg / m2. A este último grupo de pacientes se los instruye para continuar con la férula en la noche hasta un año después de la operación. Los pacientes a quienes se les permite interrumpir el uso de la férula, puede iniciar un programa de trote y ejercicios propioceptivos. Las pruebas funcionales se realizan típicamente entre los nueve y doce meses después de la operación para determinar el regreso a sus actividades completas.
Rol de la férula
Durante el tratamiento no quirúrgico y la rehabilitación postoperatoria de las lesiones del LCP, es importante mantener la articulación de la rodilla en una posición controlada que permita la curación. Si la articulación de la rodilla no está correctamente alineada durante la rehabilitación y la curación, las cargas dinámicas de los músculos isquiotibiales pueden hacer que el LCP cure elongado, lo que resulta en inestabilidad de la articulación a largo plazo.40,42 Una posición adecuadamente controlada, tal como la proporcionada por un aparato ortopédico que aplica una fuerza anterior dirigida a la tibia proximal desde posterior, puede prevenir la inestabilidad a largo plazo y mejorar los resultados. Las razones teóricas para su uso son numerosas e incluyen: 1) la protección de la reconstrucción del LCP y la prevención de la elongación del injerto después de la intervención (rehabilitación); 2) proporcionar estabilidad externa a una rodilla con LCP deficiente (funcional); y 3) mitigar el desarrollo de la artrosis en la rodilla con LCP deficiente (profiláctico).
Dado que los estudios biomecánicos demuestran que el LCP es una estructura no isométrica, con desigual tensión en todo movimiento de la rodilla,21 ha sido difícil crear una rodillera o férula que proteja el LCP durante todo el arco de movimiento de la rodilla. La mayoría de los soportes para las rodillas son “estáticas”, proporcionando la misma carga en todo el rango de flexión de la rodilla, y por lo tanto no pueden proporcionar estabilidad para la carga dinámica en vivo y mantener la tensión creada por el LCP. La férula LCP-Jack (Albrecht, Stephanskirchen, Alemania) ha demostrado previamente ser eficaz en el sostén de la tibia con una carga anterior constante.58,64 Sin embargo, es grande y voluminosa, que limita la flexión del paciente de 0° a 90° y proporciona una fuerza anterior estática en todo el rango de movimiento, que no consigue imitar la función nativa del LCP.65
Más recientemente, en una investigación in vivo de seis voluntarios varones, LaPrade y cols. Evaluaron una férula dinámica (Össur Inc., Foothill Ranch, CA, EE.UU.) que aumenta las fuerzas de forma dinámica con el aumento del ángulo de flexión en comparación con la férula de Jack, pudiendo ser óptima para la recuperación de las lesiones del LCP.66 Sin embargo, son necesarios estudios clínicos para determinar si las características de carga de la férula dinámica reproduce más de cerca el perfil de carga del LCP nativo.
RESULTADOS CLÍNICOS
Los resultados clínicos de las reconstrucciones del LCP han sido variables en la literatura. Recientemente, Spiridonov planteó la hipótesis de que pequeñas variaciones en la técnica pueden conducir a mejores resultados clínicos después de la reconstrucción con doble banda del LCP. Dado que la mayoría de las técnicas quirúrgicas dañan el vasto medial (VM) a través del uso del portal anteromedial, se puede retrasar la recuperación muscular del cuádriceps. Los autores estudiaron los efectos de un enfoque menos agresivo del VM durante la reconstrucción del LCP. Se analizaron 31 pacientes con lesiones aisladas y combinadas tratados con reconstrucción transtibial de doble banda utilizando aloinjerto de Aquiles colocado en el túnel femoral a través de un portal artroscópico lateral.58 Los injertos fueron fijados por un método interno y se pasaron distalmente a través de un túnel tibial para evitar lesiones al VM, similar a la técnica quirúrgica descrita anteriormente. Después de un período de al menos dos años, hubo mejorías significativas en las puntuaciones subjetivas y objetivas en comparación con los datos preoperatorios, así como la traducción en las radiografías con estrés, lo que sugiere que esta técnica puede tener éxito en el tratamiento de pacientes con roturas aisladas y combinados del LCP. Sin embargo, no se utilizaron grupos de control.
Además, durante la última década, se han realizado varios estudios para evaluar la eficacia de las reconstrucciones de simple versus doble banda. Hasta la fecha, la literatura no es concluyente con respecto a la superioridad de una técnica sobre la otra. Harner y cols. compararon reconstrucciones simples y dobles en un estudio biomecánico utilizando Aquiles e injertos duplicados de semitendinoso para cada técnica respectiva.52 Los autores publicaron diferencias significativas en la traslación tibial posterior en los de simple banda en comparación con la reconstrucción de doble banda y las rodillas normales, y no encontraron diferencias en la traslación entre las rodillas con doble banda y las rodillas normales. Los autores concluyeron que la reconstrucción con doble banda restauraría mejor la biomecánica de la rodilla en comparación a la simple banda en todo el rango de movimiento de la rodilla.52 En contraste, el uso de una técnica de incrustación tibial, Bergfeld y cols.67 no encontraron ninguna diferencia en la traslación en las reconstrucciones con simple o doble banda en diversos grados de flexión, concluyendo que ambas técnicas reproducen la estabilidad posterior de la rodilla.67 En su conjunto, con otros estudios publicados,68-72 existen datos contradictorios y no hay un consenso claro en la literatura de que una técnica sea preferida sobre la otra.
CONCLUSIONES
Estudios recientes que examinan las propiedades de la anatomía y la biomecánica del LCP han dado lugar a nuevas técnicas quirúrgicas de reconstrucción que intentan replicar el comportamiento funcional del LCP nativo a través del rango completo de movimiento de la rodilla. La reconstrucción con doble banda artroscópica permite la restauración de la estabilidad rotacional y posterior a través del rango completo de movimiento de la rodilla, y los estudios clínicos preliminares han demostrado resultados clínicos buenos a excelentes a corto plazo utilizando esta técnica.
Se necesitan más estudios para evaluar a fondo la eficacia clínica a largo plazo de las diversas técnicas quirúrgicas, incluyendo la simple banda frente a las técnicas de reconstrucción con doble banda y de incrustación tibial, además de sus principios de rehabilitación pertinentes, en un intento de mejorar los resultados del paciente tanto en el tratamiento quirúrgico o no de las lesiones de LCP.
BIBLIOGRAFÍA
-
Parolie JM, Bergfeld JA: Long-term results of nonoperative treatment of isolated posterior cruciate ligament injuries in the athlete. The American journal of sports medicine 1986, 14(1):35-38.
-
Torg JS, Barton TM, Pavlov H, Stine R: Natural history of the posterior cruciate ligament-deficient knee. Clinical orthopaedics and related research 1989(246):208-216.
-
Strobel MJ, Weiler A, Schulz MS, Russe K, Eichhorn HJ: Arthroscopic evaluation of articular cartilage lesions in posterior-cruciate-ligament-deficient knees. Arthroscopy : the journal of arthroscopic & related surgery : official publication of the Arthroscopy Association of North America and the International Arthroscopy Association 2003, 19(3):262-268.
-
Van de Velde SK, Bingham JT, Gill TJ, Li G: Analysis of tibiofemoral cartilage deformation in the posterior cruciate ligament-deficient knee. The Journal of bone and joint surgery American volume 2009, 91(1):167-175.
-
McAllister DR, Petrigliano FA: Diagnosis and treatment of posterior cruciate ligament injuries. Current sports medicine reports 2007, 6(5):293-299.
-
Girgis FG, Marshall JL, Monajem A: The cruciate ligaments of the knee joint. Anatomical, functional and experimental analysis. Clinical orthopaedics and related research 1975(106):216-231.
-
Harner CD, Xerogeanes JW, Livesay GA, Carlin GJ, Smith BA, Kusayama T, Kashiwaguchi S, Woo SL: The human posterior cruciate ligament complex: an interdisciplinary study. Ligament morphology and biomechanical evaluation. The American journal of sports medicine 1995, 23(6):736-745.
-
Matava MJ, Ellis E, Gruber B: Surgical treatment of posterior cruciate ligament tears: an evolving technique. The Journal of the American Academy of Orthopaedic Surgeons 2009, 17(7):435-446.
-
Makris CA, Georgoulis AD, Papageorgiou CD, Moebius UG, Soucacos PN: Posterior cruciate ligament architecture: evaluation under microsurgical dissection. Arthroscopy : the journal of arthroscopic & related surgery : official publication of the Arthroscopy Association of North America and the International Arthroscopy Association 2000, 16(6):627-632.
-
Lopes OV, Jr., Ferretti M, Shen W, Ekdahl M, Smolinski P, Fu FH: Topography of the femoral attachment of the posterior cruciate ligament. The Journal of bone and joint surgery American volume 2008, 90(2):249-255.
-
Kennedy JC, Hawkins RJ, Willis RB, Danylchuck KD: Tension studies of human knee ligaments. Yield point, ultimate failure, and disruption of the cruciate and tibial collateral ligaments. The Journal of bone and joint surgery American volume 1976, 58(3):350-355.
-
Butler DL, Noyes FR, Grood ES: Ligamentous restraints to anterior-posterior drawer in the human knee. A biomechanical study. The Journal of bone and joint surgery American volume 1980, 62(2):259-270.
-
Gollehon DL, Torzilli PA, Warren RF: The role of the posterolateral and cruciate ligaments in the stability of the human knee. A biomechanical study. The Journal of bone and joint surgery American volume 1987, 69(2):233-242.
-
Markolf KL, Slauterbeck JR, Armstrong KL, Shapiro MS, Finerman GA: A biomechanical study of replacement of the posterior cruciate ligament with a graft. Part II: Forces in the graft compared with forces in the intact ligament. The Journal of bone and joint surgery American volume 1997, 79(3):381-386.
-
Covey DC, Sapega AA, Riffenburgh RH: The effects of sequential sectioning of defined posterior cruciate ligament fiber regions on translational knee motion. The American journal of sports medicine 2008, 36(3):480-486.
-
Race A, Amis AA: The mechanical properties of the two bundles of the human posterior cruciate ligament. Journal of biomechanics 1994, 27(1):13-24.
-
Sekiya JK, Whiddon DR, Zehms CT, Miller MD: A clinically relevant assessment of posterior cruciate ligament and posterolateral corner injuries. Evaluation of isolated and combined deficiency. The Journal of bone and joint surgery American volume 2008, 90(8):1621-1627.
-
Markolf KL, Feeley BT, Tejwani SG, Martin DE, McAllister DR: Changes in knee laxity and ligament force after sectioning the posteromedial bundle of the posterior cruciate ligament. Arthroscopy : the journal of arthroscopic & related surgery : official publication of the Arthroscopy Association of North America and the International Arthroscopy Association 2006, 22(10):1100-1106.
-
Markolf KL, Zemanovic JR, McAllister DR: Cyclic loading of posterior cruciate ligament replacements fixed with tibial tunnel and tibial inlay methods. The Journal of bone and joint surgery American volume 2002, 84-A(4):518-524.
-
Kennedy NI, Wijdicks CA, Goldsmith MT, Michalski MP, Devitt BM, Aroen A, Engebretsen L, Laprade RF: Kinematic analysis of the posterior cruciate ligament, part 1: the individual and collective function of the anterolateral and posteromedial bundles. The American journal of sports medicine 2013, 41(12):2828-2838.
-
Covey DC, Sapega AA, Sherman GM: Testing for isometry during reconstruction of the posterior cruciate ligament. Anatomic and biomechanical considerations. The American journal of sports medicine 1996, 24(6):740-746.
-
Escamilla RF: Knee biomechanics of the dynamic squat exercise. Medicine and science in sports and exercise 2001, 33(1):127-141.
-
Escamilla RF, Zheng N, MacLeod TD, Imamura R, Edwards WB, Hreljac A, Fleisig GS, Wilk KE, Moorman CT, 3rd, Paulos L et al: Cruciate ligament tensile forces during the forward and side lunge. Clin Biomech (Bristol, Avon) 2010, 25(3):213-221.
-
Mesfar W, Shirazi-Adl A: Knee joint biomechanics in open-kinetic-chain flexion exercises. Clin Biomech (Bristol, Avon) 2008, 23(4):477-482.
-
Jeong WS, Yoo YS, Kim DY, Shetty NS, Smolinski P, Logishetty K, Ranawat A: An analysis of the posterior cruciate ligament isometric position using an in vivo 3-dimensional computed tomography-based knee joint model. Arthroscopy : the journal of arthroscopic & related surgery : official publication of the Arthroscopy Association of North America and the International Arthroscopy Association 2010, 26(10):1333-1339.
-
Li G, DeFrate LE, Sun H, Gill TJ: In vivo elongation of the anterior cruciate ligament and posterior cruciate ligament during knee flexion. The American journal of sports medicine 2004, 32(6):1415-1420.
-
Papannagari R, DeFrate LE, Nha KW, Moses JM, Moussa M, Gill TJ, Li G: Function of posterior cruciate ligament bundles during in vivo knee flexion. The American journal of sports medicine 2007, 35(9):1507-1512.
-
Ahmad CS, Cohen ZA, Levine WN, Gardner TR, Ateshian GA, Mow VC: Codominance of the individual posterior cruciate ligament bundles. An analysis of bundle lengths and orientation. The American journal of sports medicine 2003, 31(2):221-225.
-
Wijdicks CA, Kennedy NI, Goldsmith MT, Devitt BM, Michalski MP, Aroen A, Engebretsen L, LaPrade RF: Kinematic analysis of the posterior cruciate ligament, part 2: a comparison of anatomic single- versus double-bundle reconstruction. The American journal of sports medicine 2013, 41(12):2839-2848.
-
Moulton SG, Cram TR, James EW, Dornan GJ, Kennedy NI, LaPrade RF: The Supine Internal Rotation Test: A Pilot Study Evaluating Tibial Internal Rotation in Grade III Posterior Cruciate Ligament Tears. Orthopaedic journal of sports medicine 2015, 3(2):2325967115572135.
-
Jackman T, LaPrade RF, Pontinen T, Lender PA: Intraobserver and interobserver reliability of the kneeling technique of stress radiography for the evaluation of posterior knee laxity. The American journal of sports medicine 2008, 36(8):1571-1576.
-
Allen CR RJ, Harner CD: Posterior cruciate ligament: diagnosis and decision making. In Miller MD, Cole BJ (Eds), Textbook of Arthroscopy 2004, Elsevier.
-
Espejo-Baena A, Lopez-Arevalo R, Urbano V, Montanez E, Martin F: Arthroscopic repair of the posterior cruciate ligament: two techniques. Arthroscopy : the journal of arthroscopic & related surgery : official publication of the Arthroscopy Association of North America and the International Arthroscopy Association 2000, 16(6):656-660.
-
Kim SJ, Shin SJ, Choi NH, Cho SK: Arthroscopically assisted treatment of avulsion fractures of the posterior cruciate ligament from the tibia. The Journal of bone and joint surgery American volume 2001, 83-A(5):698-708.
-
Richter M, Kiefer H, Hehl G, Kinzl L: Primary repair for posterior cruciate ligament injuries. An eight-year followup of fifty-three patients. The American journal of sports medicine 1996, 24(3):298-305.
-
Fanelli GC, Edson CJ: Posterior cruciate ligament injuries in trauma patients: Part II. Arthroscopy : the journal of arthroscopic & related surgery : official publication of the Arthroscopy Association of North America and the International Arthroscopy Association 1995, 11(5):526-529.
-
Harner CD, Hoher J: Evaluation and treatment of posterior cruciate ligament injuries. The American journal of sports medicine 1998, 26(3):471-482.
-
Pierce CM, O’Brien L, Griffin LW, Laprade RF: Posterior cruciate ligament tears: functional and postoperative rehabilitation. Knee surgery, sports traumatology, arthroscopy : official journal of the ESSKA 2012.
-
Shelbourne KD, Jennings RW, Vahey TN: Magnetic resonance imaging of posterior cruciate ligament injuries: assessment of healing. The American journal of knee surgery 1999, 12(4):209-213.
-
Jung YB, Tae SK, Lee YS, Jung HJ, Nam CH, Park SJ: Active non-operative treatment of acute isolated posterior cruciate ligament injury with cylinder cast immobilization. Knee surgery, sports traumatology, arthroscopy : official journal of the ESSKA 2008, 16(8):729-733.
-
Shelbourne KD, Muthukaruppan Y: Subjective results of nonoperatively treated, acute, isolated posterior cruciate ligament injuries. Arthroscopy : the journal of arthroscopic & related surgery: official publication of the Arthroscopy Association of North America and the International Arthroscopy Association 2005, 21(4):457-461.
-
Shelbourne KD, Davis TJ, Patel DV: The natural history of acute, isolated, nonoperatively treated posterior cruciate ligament injuries. A prospective study. The American journal of sports medicine 1999, 27(3):276-283.
-
Shelbourne KD, Gray T: Natural history of acute posterior cruciate ligament tears. The journal of knee surgery 2002, 15(2):103-107.
-
Veltri DM, Warren RF: Isolated and Combined Posterior Cruciate Ligament Injuries. The Journal of the American Academy of Orthopaedic Surgeons 1993, 1(2):67-75.
-
Bianchi M: Acute tears of the posterior cruciate ligament: clinical study and results of operative treatment in 27 cases. The American journal of sports medicine 1983, 11(5):308-314.
-
Sekiya JK, West RV, Ong BC, Irrgang JJ, Fu FH, Harner CD: Clinical outcomes after isolated arthroscopic single-bundle posterior cruciate ligament reconstruction. Arthroscopy : the journal of arthroscopic & related surgery : official publication of the Arthroscopy Association of North America and the International Arthroscopy Association 2005, 21(9):1042-1050.
-
Mejia EA, Noyes FR, Grood ES: Posterior cruciate ligament femoral insertion site characteristics. Importance for reconstructive procedures. The American journal of sports medicine 2002, 30(5):643-651.
-
Fuss FK: Anatomy of the cruciate ligaments and their function in extension and flexion of the human knee joint. The American journal of anatomy 1989, 184(2):165-176.
-
Harner CD, Baek GH, Vogrin TM, Carlin GJ, Kashiwaguchi S, Woo SL: Quantitative analysis of human cruciate ligament insertions. Arthroscopy : the journal of arthroscopic & related surgery : official publication of the Arthroscopy Association of North America and the International Arthroscopy Association 1999, 15(7):741-749.
-
Edwards A, Bull AM, Amis AA: The attachments of the fiber bundles of the posterior cruciate ligament: an anatomic study. Arthroscopy : the journal of arthroscopic & related surgery : official publication of the Arthroscopy Association of North America and the International Arthroscopy Association 2007, 23(3):284-290.
-
Anderson C.J. ZCG, Wijkicks C.A., Engebretsen L., LaPrade R.F.: Arthroscopically pertinent anatomy of the anterolateral and posteromedial bundles of the posterior cruciate ligament. The Journal of bone and joint surgery American volume 2012, In press.
-
Harner CD, Janaushek MA, Kanamori A, Yagi M, Vogrin TM, Woo SL: Biomechanical analysis of a double-bundle posterior cruciate ligament reconstruction. The American journal of sports medicine 2000, 28(2):144-151.
-
Apsingi S, Bull AM, Deehan DJ, Amis AA: Review: femoral tunnel placement for PCL reconstruction in relation to the PCL fibre bundle attachments. Knee surgery, sports traumatology, arthroscopy : official journal of the ESSKA 2009, 17(6):652-659.
-
Dargel J, Pohl P, Tzikaras P, Koebke J: Morphometric side-to-side differences in human cruciate ligament insertions. Surgical and radiologic anatomy : SRA 2006, 28(4):398-402.
-
Cosgarea AJ, Jay PR: Posterior cruciate ligament injuries: evaluation and management. The Journal of the American Academy of Orthopaedic Surgeons 2001, 9(5):297-307.
-
Moorman CT, 3rd, Murphy Zane MS, Bansai S, Cina SJ, Wickiewicz TL, Warren RF, Kaseta MK: Tibial insertion of the posterior cruciate ligament: a sagittal plane analysis using gross, histologic, and radiographic methods. Arthroscopy : the journal of arthroscopic & related surgery : official publication of the Arthroscopy Association of North America and the International Arthroscopy Association 2008, 24(3):269-275.
-
Johannsen AM, Anderson, C.J., Wijdicks, C.A., Engebretsen, L., Laprade, R.F.: Radiographic landmarks for tunnel positioning in PCL reconstructions. The Journal of bone and joint surgery American volume 2012, In press.
-
Spiridonov SI, Slinkard NJ, LaPrade RF: Isolated and combined grade-III posterior cruciate ligament tears treated with double-bundle reconstruction with use of endoscopically placed femoral tunnels and grafts: operative technique and clinical outcomes. The Journal of bone and joint surgery American volume 2011, 93(19):1773-1780.
-
Kennedy NI, LaPrade RF, Goldsmith MT, Faucett SC, Rasmussen MT, Coatney GA, Engebretsen L, Wijdicks CA: Posterior cruciate ligament graft fixation angles, part 2: biomechanical evaluation for anatomic double-bundle reconstruction. The American journal of sports medicine 2014, 42(10):2346-2355.
-
Lopez-Vidriero E, Simon DA, Johnson DH: Initial evaluation of posterior cruciate ligament injuries: history, physical examination, imaging studies, surgical and nonsurgical indications. Sports medicine and arthroscopy review 2010, 18(4):230-237.
-
Lutz GE, Palmitier RA, An KN, Chao EY: Comparison of tibiofemoral joint forces during open-kinetic-chain and closed-kinetic-chain exercises. The Journal of bone and joint surgery American volume 1993, 75(5):732-739.
-
Watsend AM, Osestad TM, Jakobsen RB, Engebretsen L: Clinical studies on posterior cruciate ligament tears have weak design. Knee surgery, sports traumatology, arthroscopy : official journal of the ESSKA 2009, 17(2):140-149.
-
Fanelli GC: Posterior cruciate ligament rehabilitation: how slow should we go?Arthroscopy : the journal of arthroscopic & related surgery : official publication of the Arthroscopy Association of North America and the International Arthroscopy Association 2008, 24(2):234-235.
-
Jacobi M, Reischl N, Wahl P, Gautier E, Jakob RP: Acute isolated injury of the posterior cruciate ligament treated by a dynamic anterior drawer brace: a preliminary report. The Journal of bone and joint surgery British volume 2010, 92(10):1381-1384.
-
Jansson KS, Costello KE, O’Brien L, Wijdicks CA, Laprade RF: A historical perspective of PCL bracing. Knee surgery, sports traumatology, arthroscopy : official journal of the ESSKA 2012.
-
LaPrade RF, Smith SD, Wilson KJ, Wijdicks CA: Quantification of functional brace forces for posterior cruciate ligament injuries on the knee joint: an in vivo investigation. Knee surgery, sports traumatology, arthroscopy : official journal of the ESSKA 2015, 23(10):3070-3076.
-
Bergfeld JA, Graham SM, Parker RD, Valdevit AD, Kambic HE: A biomechanical comparison of posterior cruciate ligament reconstructions using single- and double-bundle tibial inlay techniques. The American journal of sports medicine 2005, 33(7):976-981.
-
Houe T, Jorgensen U: Arthroscopic posterior cruciate ligament reconstruction: one- vs. two-tunnel technique. Scandinavian journal of medicine & science in sports 2004, 14(2):107-111.
-
Wang CJ, Weng LH, Hsu CC, Chan YS: Arthroscopic single- versus double-bundle posterior cruciate ligament reconstructions using hamstring autograft. Injury 2004, 35(12):1293-1299.
-
Hatayama K, Higuchi H, Kimura M, Kobayashi Y, Asagumo H, Takagishi K: A comparison of arthroscopic single- and double-bundle posterior cruciate ligament reconstruction: review of 20 cases. Am J Orthop (Belle Mead NJ) 2006, 35(12):568-571.
-
Kohen RB, Sekiya JK: Single-bundle versus double-bundle posterior cruciate ligament reconstruction. Arthroscopy : the journal of arthroscopic & related surgery : official publication of the Arthroscopy Association of North America and the International Arthroscopy Association 2009, 25(12):1470-1477.
-
Kim YM, Lee CA, Matava MJ: Clinical results of arthroscopic single-bundle transtibial posterior cruciate ligament reconstruction: a systematic review. The American journal of sports medicine 2011, 39(2):425-434.